1 Agtergrond van die dengue-epidemie: 'n Toenemende wêreldwye uitdaging vir openbare gesondheid
Dengue is 'n akute muskietgedraagde virussiekte wat veroorsaak word deur die dengue-virus (DENV), wat na vore gekom het as die vinnigste verspreide arbovirussiekte wêreldwyd en 'n aansienlike bedreiging vir openbare gesondheidsveiligheid inhou. Oor die afgelope twee dekades het die wêreldwye voorkoms van dengue dramaties toegeneem, met die aantal aangemelde gevalle wat jaarliks verdubbel sedert 2021 [1]. In Desember 2023 het die Wêreldgesondheidsorganisasie (WGO) 'n wêreldwye dengue-noodtoestand verklaar om gekoördineerde internasionale reaksiepogings te versterk. Epidemiologiese ramings van die WGO dui daarop dat ongeveer 3,9 miljard individue wêreldwyd 'n risiko loop vir dengue-infeksie, met 'n geraamde 390 miljoen infeksies wat jaarliks voorkom - waarvan 96 miljoen as klinies duidelike gevalle voorkom [1,2].
2 Epidemiologiese Hoogtepunte
Die epidemiologiese eienskappe van dengue word gevorm deur die interaksie van virologiese faktore, vektorekologie, immuunresponse van die gasheer en sosio-omgewingstoestande. 'n Omvattende begrip van hierdie eienskappe is noodsaaklik vir die ontwikkeling van effektiewe voorkomings- en beheerstrategieë sowel as akkurate diagnostiese benaderings.
2.1 Transmissievektore en Stedelike Transmissiepatrone
Dengue-virus word hoofsaaklik oorgedra deurAedes aegypti en Aedes albopictusmuskiete. Onder hierdie vektorspesies word Aedes aegypti erken as die mees kritieke transmissievektor, gekenmerk deur hoë "menslike aanpasbaarheid" en wydverspreide verspreiding in tropiese en subtropiese stedelike omgewings. Anders as ander muskietvektore van arbovirale patogene, vertoon Aedes aegypti die volgende belangrike epidemiologiese eienskappe:
-'n Voorkeur vir teling in antropogeniese omgewings (bv. waterbergingshouers, weggooibande)
-'n Sterk tropisme vir menslike bloed as 'n voedingsbron
-Voedingsgedrag gedurende die dag
Hierdie eienskappe definieer dengue as 'n tipiese"stedelike aansteeklike siekte,"met transmissie-effektiwiteit aansienlik verhoog in digbevolkte gebiede. WGO-verwante studies het getoon dat in hoë-digtheid stedelike omgewings, verhoogde frekwensie van muskiet-mens kontak die basiese reproduksiegetal (R₀) van DENV aansienlik kan verhoog, en sodoende die verspreiding van epidemies versnel [2].
2.2 Globale verspreidingstendense en dryfvere
Volgens WGO-verslae het die wêreldwye aantal aangemelde dengue-gevalle eksponensieel toegeneem oor die afgelope twee dekades [1,3]. Hierdie opwaartse tendens word hoofsaaklik gedryf deur die volgende onderling gekoppelde faktore:
(1) Klimaatsverandering: Stygende globale temperature brei nie net die geografiese reeks geskikte habitats vir muskietvektore uit nie, maar verkort ook die ekstrinsieke inkubasietydperk van DENV binne die muskietgasheer, wat die oordragdoeltreffendheid verbeter. Klimaatgeïnduseerde variasies in muskietdigtheid is deur die WGO bekragtig as 'n betroubare voorspeller van die ruimtelike en tydelike dinamika van dengue-uitbrake.
(2) Verstedeliking: Vinnige en onbeplande stedelike uitbreiding het oorvloedige teelhabitatte vir muskietvektore geskep, terwyl verhoogde bevolkingsdigtheid die kontinuïteit van DENV-oordragkettings versterk het.
(3) Globale Bevolkingsbeweging: Internasionale reise en handel het die vinnige grensoverschrijdende oordrag van DENV vergemaklik, wat die oorgang van ingevoerde gevalle na volgehoue plaaslike oordrag bevorder het. WGO-moniteringsdata toon dat die Verenigde State tussen 2010 en 2021 7 528 reisverwante dengue-gevalle aangemeld het, waarvan 3 135 hospitalisasie vereis het en 19 tot mortaliteit gelei het.
(4) Uitbreiding van vektorverspreiding: Wêreldwyd brei die geografiese verspreiding van Aedes aegypti en Aedes albopictus steeds uit, met Aedes-muskiete wat toenemend in dele van Europa gevestig word. Gevolglik het dengue ontwikkel van 'n tradisioneel streeksepidemie tot 'n wêreldwye bedreiging vir die openbare gesondheid.
2.3 Multi-serotipe ko-sirkulasie en herinfeksiemeganismes
Dengue-virus bestaan uit vier antigenies verskillende serotipes (DENV-1 tot DENV-4). Infeksie met een serotipe verleen langtermyn beskermende immuniteit teen daardie spesifieke serotipe, maar slegs tydelike en gedeeltelike kruisbeskerming teen die ander drie serotipes. Die algemene bevolking is universeel vatbaar vir DENV, met slegs 'n subgroep van besmette individue wat kliniese siekte ontwikkel [2].
In endemiese streke sirkuleer verskeie DENV-serotypes dikwels gelyktydig, wat die potensiaal het vir individue om verskeie dengue-infeksies gedurende hul leeftyd te ervaar. WGO-epidemiologiese studies het multi-serotype-ko-sirkulasie as 'n sleuteldrywer van periodieke dengue-uitbrake geïdentifiseer [1].
2.4 Sekondêre infeksie en teenliggaamafhanklike versterking
'n Kritieke en unieke verskynsel in dengue-epidemiologie isteenliggaam-afhanklike versterking (ADE)Tydens sekondêre infeksie met 'n heteroloë DENV-sertipe, vergemaklik nie-neutraliserende teenliggaampies wat tydens die primêre infeksie geproduseer word, virale toegang tot monosiete en makrofage, waardeur virale replikasie verbeter word. Hierdie meganisme word wyd deur die WGO erken as 'n belangrike patogene faktor in ernstige dengue, insluitend dengue hemorragiese koors en dengue-skoksindroom [1].
WGO-epidemiologiese data toon konsekwent dat individue met sekondêre dengue-infeksie 'n aansienlik hoër risiko het om ernstige siekte te ontwikkel in vergelyking met diegene met primêre infeksie - 'n kenmerk wat van groot belang is vir siektemonitering en kliniese bestuur. Dit is belangrik om daarop te let dat terwyl die risiko van ernstige siekte verhoog word tydens sekondêre infeksie, infeksie met enige DENV-serotype moontlik tot ernstige dengue kan vorder [1].
2.5 Nie-spesifieke kliniese manifestasies en risiko van verkeerde diagnose
Die kliniese manifestasies van dengue is opvallend nie-spesifiek, veral in die vroeë stadiums van die siekte, en oorvleuel dikwels met dié van ander muskietgedraagde virusinfeksies (bv. chikungunya- en Zika-virusse) sowel as sekere respiratoriese infeksies. WGO-ramings dui daarop dat 40-80% van DENV-infeksies asimptomaties is [3].
Tipiese kliniese manifestasies sluit in:
-Akute koors (wat vir 2-7 dae aanhou, wat tweefasig kan wees)
-Erge hoofpyn en retro-orbitale pyn (pyn agter die oë)
-Spier- en gewrigspyn (algemeen bekend as "beenbreukkoors")
-Makulêre of makulopapulêre uitslag
-Ligte hemorragiese manifestasies (bv. ekchimose, epistaksis, tandvleisbloeding)
Simptomatiese dengue word tipies in drie afsonderlike fases verdeel: die koorsfase, die kritieke fase en die herstelfase. Ongeveer minder as 5% van simptomatiese pasiënte vorder tot ernstige dengue. As gevolg van die gebrek aan spesifieke kliniese kenmerke, is diagnose gebaseer op slegs kliniese simptome uitdagend, wat die risiko van verkeerde diagnose en onderdiagnose verhoog. Die WGO beklemtoon eksplisiet dat kliniese diagnose alleen onvoldoende is om akkuraatheid te verseker, wat laboratoriumbevestiging onontbeerlik maak [1].
3 Sleutelpunte van die WGO “Laboratoriumtoetsing vir Dengue-virus: Tussentydse riglyne, April 2025″
In April 2025 het die Wêreldgesondheidsorganisasie opgedateerde tussentydse riglyne oor laboratoriumtoetse vir DENV vrygestel, wat gesaghebbende tegniese riglyne vir globale dengue-diagnose bied. Hierdie riglyne sintetiseer die nuutste bewyse oor dengue-laboratoriumtoetse in die konteks van die voortdurende globale dengue-noodtoestand en bied praktiese aanbevelings wat aangepas is vir omgewings met verskillende hulpbronvlakke.

3.1 Fundamentele Beginsels van Toetsstrategie
Die riglyne beklemtoon dat dengue-diagnose 'n multimerker-gekombineerde toetsstrategie gebaseer op die stadium van die siekte moet aanneem [1]. Gegewe die afwesigheid van 'n universele diagnostiese algoritme, moet toetsstrategieë aangepas word by plaaslike epidemiologiese kontekste, met inagneming van die volgende sleutelfaktore [1]:
-Infeksiestadium: Die aantal dae na die aanvang van die simptoom bepaal die mees geskikte toetsmetode.
-Monstertipe: Die geskiktheid van volbloed, plasma of serum vir DENV-opsporing
-Streeksepidemiologie: Die plaaslik sirkulerende DENV-serotipes en ko-sirkulasie van ander arbovirusse
-Ko-infeksierisiko: In streke met oorvleuelende arbovirus-sirkulasie, moet multiplekstoetsing oorweeg word om tussen verskillende patogene te onderskei.
3.2 Stadiumgebaseerde Toetsstrategie
Volgens die WGO-riglyne moet dengue-laboratoriumtoetse duidelike tydvensters volg gebaseer op die stadium van siekte [1,2]:
(1) Akute Fase Toetsing (≤7 dae na aanvang)
-Nukleïensuurtoetsing (Molekulêre toetsing): Omgekeerde transkripsie-polimerase-kettingreaksie (RT-PCR) en ander molekulêre metodes bespeur DENV RNA met hoë sensitiwiteit.
-Antigeentoetsing: NS1-antigeenopsporing, wat binne 1-3 dae na aanvang opspoorbaar word.
Gedurende die akute fase is viremievlakke relatief hoog, en nukleïensuur- en antigeentoetse bereik optimale sensitiwiteit.
(2) Herstelfasetoetsing (≥4 dae na aanvang)
-Serologiese toetsing: IgM-teenliggaampies word tipies opspoorbaar rondom dag 4 na aanvang.
In die meeste gevalle bly IgM-teenliggaampies vir 14-20 dae aanhou, en in sommige gevalle kan die aanhoudendheid tot 90 dae duur.
-IgG-toetsing het beperkte waarde vir akute dengue-diagnose as gevolg van potensiële kruisreaktiewe teenliggaampies van vorige flavivirusinfeksie of inenting.
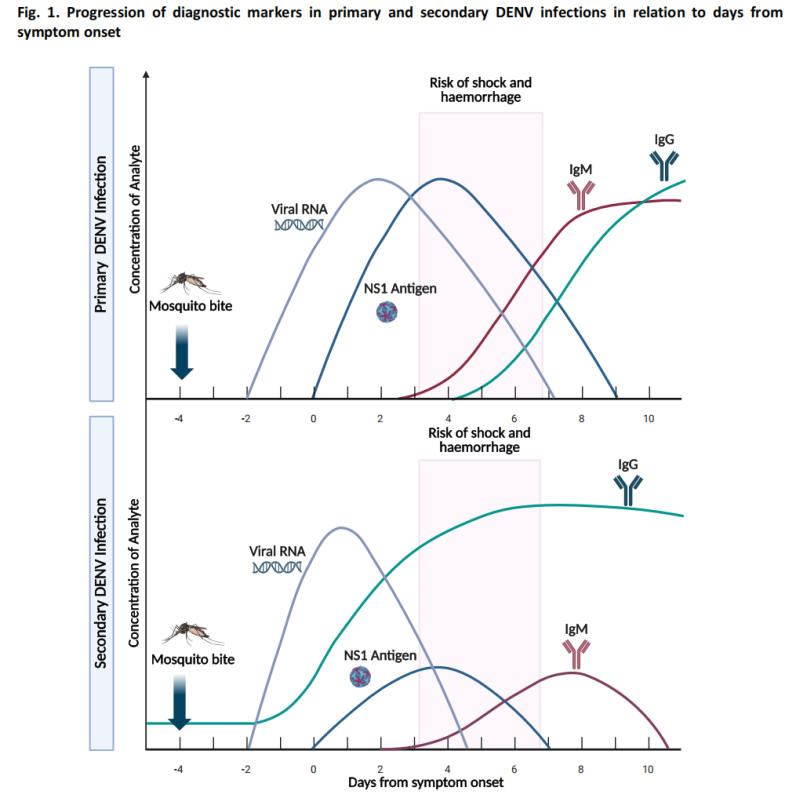
(3) Diagnostiese Algoritme vir Verdagte Gevalle
Die riglyne sluit 'n diagnostiese algoritme vir vermoedelike dengue-gevalle in, en beveel gepaste toetsmetodes aan gebaseer op dae na die aanvang van simptome: NS1-antigeentoetsing en nukleïensuurtoetsing is die primêre benaderings in die vroeë fase, terwyl serologiese toetsing die primêre metode in die latere fase is.
3.3 Toetsmetode-prestasie-evaluering en -keuse
Volgens die WGO is 'n sistematiese evaluering van die prestasie en toepaslike scenario's van verskeie dengue-toetse soos volg:
| Toetsmetode | Teiken | Tydvenster | Primêre Toepassingscenario | Oorwegings |
| Nukleïensuurtoetsing | Virale RNA | 1-7 dae na aanvang | Vroeë bevestiging, serotipe-identifikasie | Goue standaardmetode; vereis gespesialiseerde laboratoriumtoerusting en tegniese kundigheid |
| NS1 Antigeentoetsing | Nie-strukturele proteïen | 1-3 dae na aanvang | Vroeë vinnige sifting | Beskikbaar in vinnige diagnostiese toets (RDT) formaat, geskik vir hulpbronbeperkte omgewings |
| IgM-teenliggaamtoetsing | Spesifieke IgM-teenliggaampies | ≥4 dae na aanvang | Diagnose van onlangse infeksie | 'n Enkele serummonster dui slegs op 'n moontlike onlangse infeksie; serokonversie is nodig vir bevestiging. |
| IgG-teenliggaamtoetsing | Spesifieke IgG-teenliggaampies | Herstellende/vorige infeksie | Epidemiologiese ondersoek, assessering van immuniteitstatus | 'n Enkele serummonster is nie geskik vir akute dengue-diagnose nie |
| Gekombineerde toetsing (NS1+IgM/IgG) | Antigeen + Teenliggaampies | Volledige siekteverloop | Omvattende diagnose van dengue-infeksie | Tans die beste presterende RDT-formaat vir dengue-diagnose |
| NGS | Virale RNA | 1-7 dae na aanvang | Virale genomiese toesig | Vereis gespesialiseerde volgordebepalingstoerusting en bioinformatika-analisevermoëns |
4 Makro- en Mikrotoets Dengue-opsporingsproduk-aanbevelings per scenario
Om dengue-voorkoming en -beheer te ondersteun, bied Macro & Micro-Test 'n geïntegreerde diagnostiese portefeulje wat vinnige sifting, molekulêre bevestiging en genomiese toesig dek, wat aan behoeftes oor verskillende stadiums van uitbrekingsbestuur voldoen.
4.1 Scenario 1: Vinnige Sifting en Gerigte Toesig
Van toepassing op koorsklinieke, primêre gesondheidsorgfasiliteite, gemeenskapsondersoeke vir uitbrekings en hawe-/grenskwarantyn.
-Dengue-virus NS1-antigeen-sneltoets: Bespeur vroeë infeksie (1-3 dae na aanvang) met 15-minuut-resultate vir vinnige triage.
-Dengue-virus IgM/IgG-teenliggaamtoets: Onderskei primêre/sekondêre infeksies om ernstige siekterisiko te evalueer.
-Dengue-virus NS1-antigeen + IgM/IgG-gekombineerde vinnige toets: Bespeur gelyktydig antigeen en teenliggaampies vir volledige diagnose.
-Chikungunya-virus IgM/IgG-teenliggaamtoets: Maak differensiële diagnose met dengue moontlik om patogene akkuraat te identifiseer.
4.2 Scenario 2: Presisiediagnose en noodreaksie
-Dengue-virus I/II/III/IV Nukleïensuur-opsporingstel: Bespeur en onderskei 4 serotipes (opsporingslimiet 500 kopieë/ml) vir die opsporing van uitbrekings.
-Gevriesdroogde Dengue-virus PCR-stel: Vervoerbaar by kamertemperatuur, geskik vir gebiede met beperkte hulpbronne en skielike uitbrake.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Bespeur gelyktydig 3 arbovirusse vir doeltreffende differensiële diagnose in komplekse uitbrake.

Al die bogenoemde reagense is versoenbaar met die AIO 800 Volledig Geoutomatiseerde Monster-tot-Antwoord-Sisteem, wat handmatige werking en kruiskontaminasie verminder, en doeltreffendheid en bioveiligheid verbeter.
4.3 Scenario 3: Genomiese toesig en virale afstammingsanalise
Van toepassing op nasionale verwysingslaboratoriums, openbare gesondheidsnavorsingsinstellings, in lyn met die WGO se posisionering van NGS.
Macro & Micro-Test se genomiese toesigoplossings ondersteun volledige genoomvolgordebepaling vir virusopsporing, oordragkettingverduideliking, variantmonitering en aanpassing van entstofstrategie. Hulle ondersteun handmatige/outomatiese werkvloei, wat deurset en reproduceerbaarheid verbeter, wat laboratoriums in staat stel om op te gradeer van roetinetoetsing na gevorderde toesig, in ooreenstemming met die WGO se klem op die versterking van virale evolusiemonitering.

4.4 Waarde van Geïntegreerde Oplossings
Makro- en Mikrotoets bied volledige diagnostiese oplossings vir die opsporing van arbovirusse, wat elke stadium van uitbrekingsbestuur ondersteun: vinnige siftingsinstrumente vir gesondheidsorginstellings in die voorste linie, molekulêre bevestiging vir presisiediagnose, en heelgenoom-analisevermoëns vir epidemiologiese toesig. Met hoëprestasie-toetse, buigsame werkvloeie en outomatiseringsgereed platforms, bemagtig hierdie oplossings laboratoriums en openbare gesondheidstelsels om voorbereiding en reaksie op opkomende arbovirusbedreigings wêreldwyd te versterk.
Verwysings
[1] Wêreldgesondheidsorganisasie. Laboratoriumtoetsing vir Dengue-virus: Tussentydse riglyne, April 2025. Genève: Wêreldgesondheidsorganisasie; 2025.
[2] WGO Globale Arbovirus-inisiatief Tegniese Adviesgroep. Versterking van Globale Gereedheid en Reaksie op Arbovirussiektebedreigings: 'n Oproep tot Aksie. Lancet Infect Dis. 2026;26(1):15-17.
[3] Die Lancet-mikrobe. Oorkoming van die dilemma van dengue-diagnostiek. Lancet-mikrobe. 2025;6(7):101190.
Plasingstyd: 20 Maart 2026
